今回は、私の大好きな電解質で悪性腫瘍患者の低マグネシウム血症について触れたい。
今回は、導入編として一般的な話を記載していく。
定義:低マグネシウム血症:血清Mg<1.8mg/dl
悪性腫瘍、入院中や集中治療患者では50-60%程度とリスクが上昇する(Journal of intensive ar 2018)。
低マグネシウム血症は急性であろうが慢性であろうが臨床的予後の悪化と関連している。慢性の低マグネシウム血症はインスリン抵抗性、糖尿病、糖尿病性腎症の悪化の促進と関連している。
低マグネシウムの重症度と症状:
Grade1:血清Mg:1.2-1.7mg/dl 倦怠感や症状がない
Grade2:血清Mg:0.9-1.2mg/dl 筋力低下、繊維側筋攣縮
Grade3:血清Mg:0.7-0.9mg/dl 神経学的所見の出現、心房細動
Grade4:血清Mg:0.7mg/dl 未満 痙攣、テタニー、眼振、精神疾患、致死的不整脈
Mgの分布やバランスについて
Mgは大人では平均24gあり、99%が細胞内(骨、筋肉、軟部組織)に分布。30%が蛋白(主にアルブミン)と結合している。
マグネシウムはナッツ(アーモンド)や緑黄色野菜(ほうれん草、ふだん草など)、シリアルやミルクやヨーグルトに多く含まれる。
・消化管から120mg/day吸収され、20mg/day分泌される。
消化管吸収は通常は30-50%程度だが、低マグネシウム下であれば吸収が80%まで増加する。
・腎臓からは約2400mg/day濾過され、2300mg/day再吸収されnet excretion は100mg/dayになる。
低マグネシウム下であれば、net excretionが12mg/day未満になる。
□消化管吸収は2パターンある。
・Paracellular route:受動的なメカニズムでMg吸収の90%を担っている。Tight junctionの部分のClaudinによって調整されている。腸管にはClaudin2,7,12が発現している。小腸から盲腸まではこのルートで吸収している。
・Transcellular route:結腸ではこの方法で吸収される。TRPM6,7が活性され、吸収される。
□腎臓での吸収
・蛋白結合のないMgは糸球体を自由に通過する。
・近医尿細管で15%が再吸収され、ヘンレの太い上行脚(TAL)で大部分(70%)再吸収され、遠位尿細管で10%が再吸収される。
TALで再吸収の主体になるのがClaudin16,19であり、Paracellular routeで再吸収を行なっている。
図に示したようにClaudin14はClaudin16にnegativeに働き、CaやMgなどの陽イオンの再吸収を減少させる。
TALのCaSR(Calcium sensing receptor)活性化によって、NKCC2 (Na-K-2 Chloride Cotransporter) やROMK (Renal Outer Medullary K)の抑制によってMgやCaの再吸収を抑制される。また、Claudin14発現を調整させ、miR-9・miR-374のmicroRNAの発現を低下させることで、Ca・Mgの再吸収を低下させる。
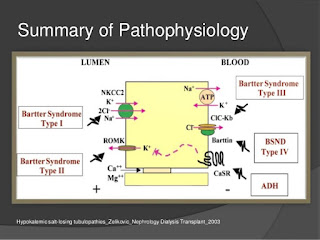
*少し脱線:ここで、NKCC2、ROMK、CIC-Kb、Barttinの遺伝子の変異は、それぞれBartter症候群type1、type2、type3、type4と呼ばれ、これらは低マグネシウム血症を特徴としている。しかし、中には低マグネシウムを来さないものもあり、これは代償性にDCT (Distal Convoluted Tubule:遠位曲尿細管)での再吸収が亢進している。CIC-Kb、Barttinは DCTにも発現しているため低マグネシウム血症は来さない場合が多い。下表参照。
本題に戻って、下の図には記載していないが、Claudin10もTALでの陽イオン選択性に非常に重要な役割を果たしている。動物実験で同様にClaudin10ノックアウトマウスが、高マグネシウム血症・尿路結石・Na再吸収障害を生じていることがわかった。これは、Claudin10がないことで、TALでのCaとMgの再吸収がしやすくなる。
また、DCT (Distal Convoluted Tubule:遠位曲尿細管)もMgにおいて重要な役割をはたす。Mg再吸収においては10%を担う。
DCTにおいては、TRPM6 Mg channelを介して、transcellular routeで再吸収される。インスリンとEGFはTRPM6の発現を増加させる。
NCC (Na-Cl Cotransporter)もDCTでのMg再吸収に関わる。
Gitelman 症候群(NCCの変異)は正常血圧、低カリウム血症、代謝性アルカローシス、低マグネシウム血症が特徴である(上表参照)。NCCノックアウトマウスではTRPM6の発現が低下しすることから、Gitelman症候群での低マグネシウム血症は、再吸収の障害での尿中排泄とわかる。 DCTのTRPM6を介しての再吸収は電気的な差で生じる。Kv1.1(voltage-gated K channel)が電気的差の形成で重要である。
今回は、まずは低マグネシウム血症の導入編という形で話をしてみた。また、次回に悪性腫瘍との関連の話を進めていければと思う。