膜性腎症に対するリツキシマブの有効性を示すMENTOR試験が発表されたのは、2019年。その2年後には、2021年版KDIGO腎炎・ネフローゼガイドラインで膜性腎症の第一選択薬の一つになった。
ということはそろそろ、先を行く薬が登場しているころかな・・と思ったら、オビヌツズマブとリツキシマブを比較する中国の一施設試験がCJASNに発表されていた(DOI: 10.2215/CJN.0000000000000555)。
ヒト化タイプII抗CD20モノクローナル抗体オビヌツズマブ(商品名ガザイバ®)は、タイプI抗CD20モノクローナル抗体のリツキシマブと異なるエピトープを認識して、より効率にB細胞をアポトーシスに至らせる。
そして、Fc部分についた糖鎖(フコース)を極力減らすことで、Fc受容体を介したナチュラルキラー細胞による細胞傷害やマクロファージによる貪食が起きやすくなっている。
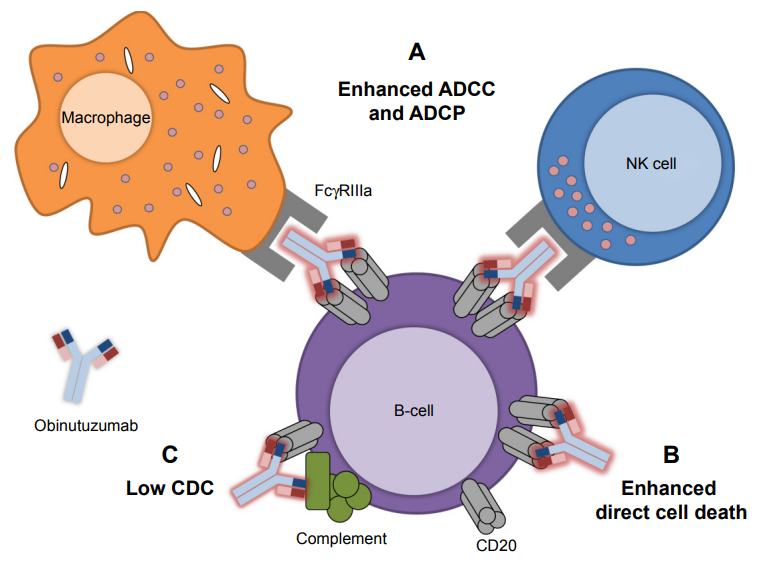 |
| (出典はDrug Design Development and Therapy 2017 11 295) |
もちろんリンパ腫に対して開発された薬だが(日本でも2018年に承認された)、リツキシマブと同様に免疫疾患にも試されている。
腎臓内科領域では、ループス腎炎に対するプラセボ対照の第2相試験NOBILITYが2022年に発表され(Ann Rheum Dis 2022 81 100)、ステロイド+MMFに追加した介入群は対照群にくらべて104週の完全腎寛解(蛋白尿<0.5g/gCr、正常腎機能、尿RBC 10/hpf未満)の割合が有意に高かった。
膜性腎症についてはRTX不応・不耐例に試された一施設試験が2020年に発表され(KI Reports 2020 5 1510)、蛋白尿の改善を認めた。
 |
| 出典は前掲KI Reports |
そして今回の試験では、ACEI/ARBにかかわらず蛋白尿が3.5g/gCr以上(平均約8g/d)でeGFR 30ml/min/1.73m2以上(平均約100ml/min/1.73m2)の原発性膜性腎症患者をオビヌツズマブ群21例、リツキシマブ群42例にランダム化した。
リツキシマブは375mg/m2を週1回×4(非寛解例は6ヵ月後に再投与:約80%が再投与された)、オビヌツズマブは1gを2週間あけて2回(再投与はなし)のレジメンだった。どちらも初回投与時のみソルメドロール40mgが、そしてすべての投与時にクロルフェニラミン10mgとアセトアミノフェン500mgが前投薬された。
結果、12か月後の完全寛解(蛋白尿<0.3g/gCrかつ腎機能低下なし)はオビヌツズマブ群の38%、リツキシマブ群の14%にみられた(p=0.04)。不完全寛解を含むプライマリ・アウトカムはオビヌツズマブ群の95%、リツキシマブの67%にみられた(p=0.03)。
また、PLA2R関連原発性膜性腎症に限ると、PLA2R<2RU/mlの免疫学的寛解はオビヌツズマブの93%、リツキシマブの73%にみられ(p=0.11)、寛解例ではほとんどが6ヵ月後の時点でCD19陽性B細胞が血中からdepleteされていた。
安全性については、重度の有害事象は両群とも報告されず、感染症(約20%)、infusion-related reactions(約6%)は両群でほぼ同じ割合で、いずれも軽症だった。
「どうせやるならとことん」という感じである。B型肝炎の活性化とPMLがFDAのblack box warningになっているが、これらはリツキシマブにおいても懸念されていたことであり、少なくとも前掲試験では有害事象に差は見られなかった(ただし、両群ともHBV抗体陽性のキャリア例はエンテカビル、潜在結核例はイソニアジドが投与されていた)。
身近なところでも、移植後FSGS再発など、少しずつリツキシマブ不応例に試されて始めている。臨床現場にいると「今の薬がだめでも次の薬があります」と言えることは医師と患者両方にとって心の支えになる。リツキシマブの次世代薬として、今後オビヌツズマブ(筆者はオビと略しているが)を目や耳にする機会は増えていくと思われる。